11月4日に厚生労働省はロナプリーブ®点滴静注の効能効果、用法用量について一部変更を特例承認することを決定しました。これによりロナプリーブ®の適応や使い方の幅が広がることになります。今回はロナプリーブ®が特例承認によりどう変わるかを見ていきたいと思います。
ロナプリーブ®について簡単におさらいしましょう。
ロナプリーブ®は新型コロナウイルスに対する2種類の抗体であり、これによりウイルスの感染能力を阻害します。
詳しくは以前に書いた記事をご覧ください。 ⇒ ロナプリーブ点滴静注
今回の変更点を見てみましょう。
・予防的使用が可能となる
今までのロナプリーブ®の適応は「SARS-CoV-2 による感染症」でした。(SARS-CoV-2とは新型コロナウイルスのことです)
しかし今回の特例承認で適応は「SARS-CoV-2 による感染症及びその発症抑制」になりました。治療だけでなく予防的使用が可能となります。
ただし全ての人に使用できるわけではありません。以下の条件を全て満たした場合のみ使用可となります。
・感染症患者の同居家族又は共同生活者等の濃厚接触者、又は無症状の病原体保有者
・重症化リスク因子を有する
・ワクチン未接種者、又はワクチン接種歴を有する場合でその効果が不十分と考えられる
実際に使用できる人はかなり限られそうです。しかし重症化リスクの高い人を未然に救える可能性が高くなるのでこれだけでも価値はありそうですね。
なお「ワクチン接種歴を有する場合でその効果が不十分と考えられる者」の範囲については、抗がん剤や免疫抑制剤を使用している、骨髄や臓器移植をしている、末期腎不全、肝硬変などがあげられます。
・皮下注射が可能となる
今までの使用法は静脈への点滴だけでした。しかし今回の特例承認で皮下注射が可能になりました。これに伴いロナプリーブ®の名称も「ロナプリーブ点滴静注セット」から「ロナプリーブ注射液セット」に変わりました。
皮下注射が可能になりましたが、基本的には点滴静注で使用することになります。
添付文書でも用法及び用量に関する注意の項目に
「点滴静注により投与すること。点滴静注による投与が実施できずやむを得ない場合にのみ皮下注射による投与を検討すること。臨床試験において皮下注射による投与時の有効性は確認されていない。」
と記載されています。
「皮下注射による投与時の有効性は確認されていない」と書くのはやりすぎな気もしますが、実際には臨床試験データが限られているためだからだそうです。
「点滴静注による投与が実施できずやむを得ない場合」とは血管確保が困難な場合などがこれにあたります。
点滴静注の場合はカシリビマブとイムデビマブそれぞれ600mg(5mL)を点滴バックに混合して単回で点滴静注していました。
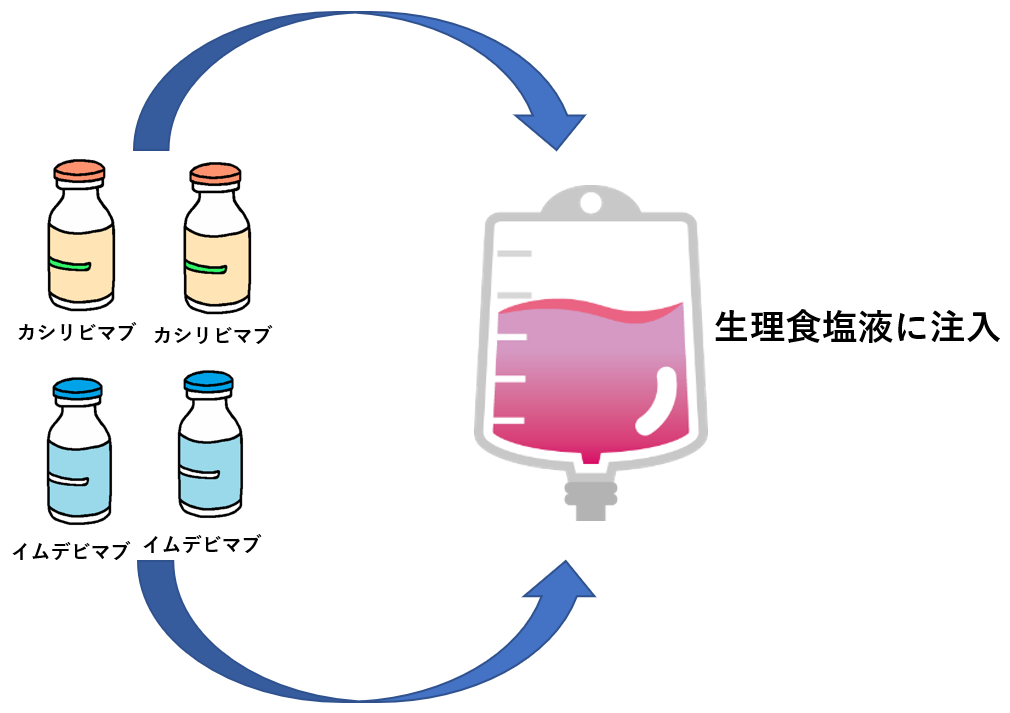
しかし皮下注射する場合はカシリビマブとイムデビマブを混合しません。それぞれを2.5mLシリンジに2本ずつ、計4本を皮下注射することになります。
※カシリビマブ同士、イムデビマブ同士を混合して5mLにもしません。2.5mLシリンジを全部で4本、それぞれ別々の箇所に皮下注射します。

注射部位は腹部、大腿部、上腕部のいずれかです。同じ箇所に繰り返し注射はせずに、それぞれの注射部位から少なくとも5cm離して投与します。
今回の特例承認でロナプリーブ®が使えるケースが多少多くなりましたが、まだまだ制限が多いですね。個人的には抗体カクテル療法は現在の新型コロナウイルス治療では最も効果の高いものと思っています。もっと手軽に使えるようになるか、劇的な効果のある新たな治療薬が早く出てきて欲しいものです。
にほんブログ村
記事が良かったと思ったらランキングの応援をお願いします。



コメント